21. Aşağıda oda koşullarında bir asit-baz tepkimesi verilmiştir. NH3(suda) + HCl(suda) - NH4Cl(suda) Kayıf baz Kuvvetli asit Tuz Buna göre, tepkimede oluşan tuz ile ilgili I. Anyonu hidrolize uğrar. Tuz çözeltisinin pH

AYT Kimya Konu Anlatım Modülleri Modül 4 Kimyasal Tepkimelerde Denge Sulu Çözeltilerde Denge (Asitler ve Bazlar) Çözünme - Çökelme Dengeleri - Yalnız iii-Kİmyasal tepkİmelerde denge-Sulu ÇÖzeltİ dengelerİ | PubHTML5

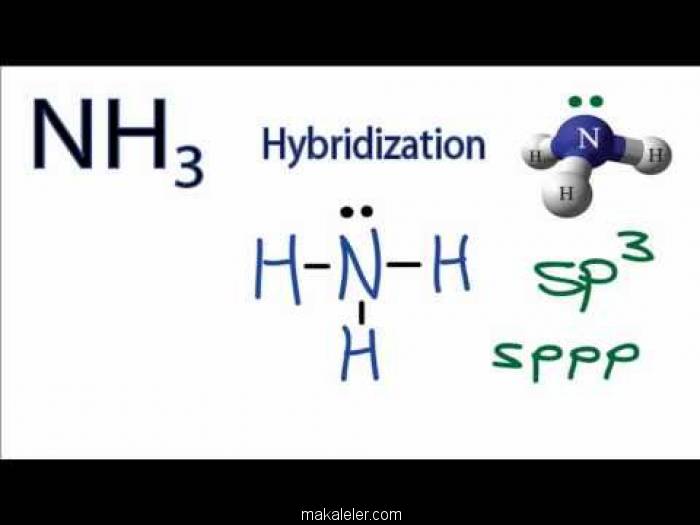
3. Amonyak (NH3) suda iyonlaşarak çözünebilmektedir. Ancak iyonlaşma oranı düşüktür. Amonyağın sulu çözeltisi dikkate alındığında; alwol 1. Dipol-dipol minste II. İyon- dipol III. London IV. Hidrojen Bağı etkileşimlerinden ması beklenir? A) I
NH3 (Amonyak) asit mi baz mı? NH3 asidik mi bazik mi? Amonyak suda çözünür mü, hangi özelliği gösterir? - Haberler

AYT Kimya Konu Anlatım Modülleri Modül 4 Kimyasal Tepkimelerde Denge Sulu Çözeltilerde Denge (Asitler ve Bazlar) Çözünme - Çökelme Dengeleri - Yalnız iii-Kİmyasal tepkİmelerde denge-Sulu ÇÖzeltİ dengelerİ | PubHTML5

11. NH319) H2O() Amonyak gazı ve suda çözünmesi ile ilgili aşağıdaki yargılardan hangisi vanlıştır? A)

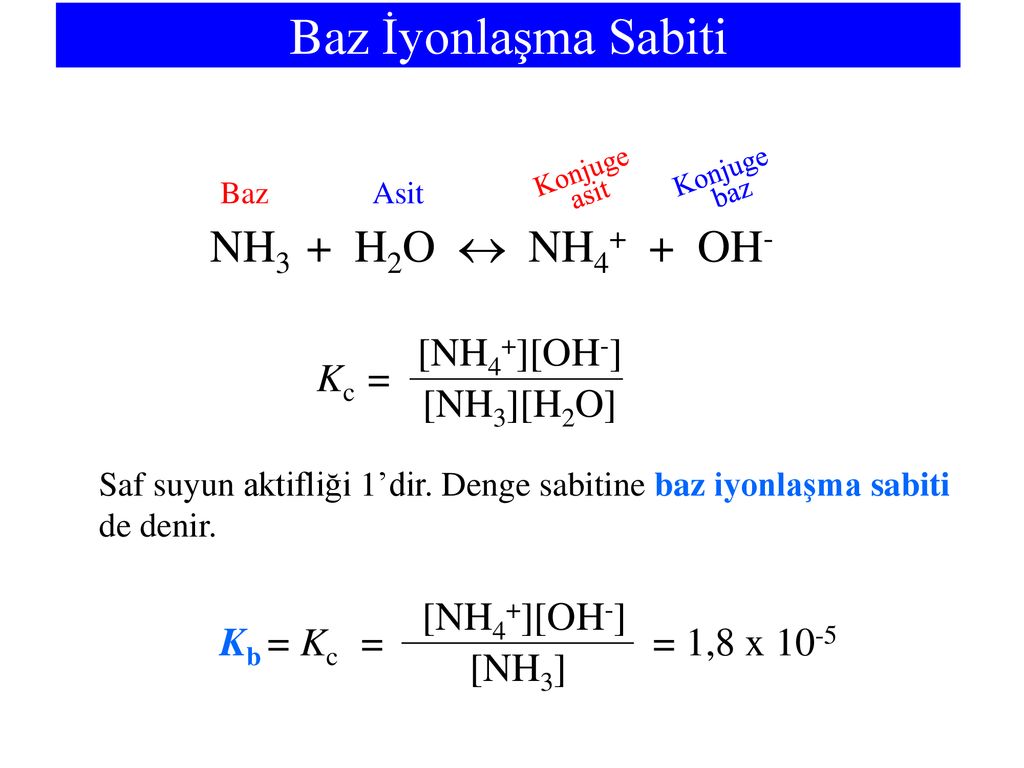
NH3(suda) + H2O(s) = NH4+(suda) + OH-(suda) NH3ün saf sudaki iyonlaşma denklemi yukarıda verilmiştir. Buna göre, oda koşullarında 0,5 mol NH3 ün suda çözülmesiyle hazırlanan 5 litrelik sulu çözeltisinde NH3 ün iyonlaşma

6. 0,1 mol NH3 ve 0,1 mol NH4Cl yeterli miktarda arı suya konarak 1 litrelik çözelti hazırlanıyor. (NHACI suda NH4* ve Cl" iyonlarına tam olarak ayrışır.) Buna göre hazırlanan çözeltiyle ilgili aşağıdakiler

6. Amonyak (NH3) suda çözündüğü zaman amon- yum (NH) ve hidroksit (OH) iyonlarına ayrış- maktadır. Buna göre, I. NH3 bazik özelliktedir. II. NH, çözeltisi mavi turnusol kâğıdını kırmızıya çevirir. III. NH, çözeltisinin

16 Amonyağın su ile olan tepkimesi aşağıdaki gibidir. NH3(suda) +H2O(s) =NHA(suda) + OH 4 (suda) Buna göre, amonyağın sulu çözeltisiyle ilgili, I. Bazik özellik gösterir. II. pH değeri 7'den küçüktür. X X